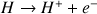Introduction
Une réaction acido-basique au sens de Brönsted met en jeu un transfert de protons
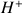 entre ses réactifs. Les réactifs sont un acide d'un premier couple acide/base et une base d'un autre couple acide/base.
entre ses réactifs. Les réactifs sont un acide d'un premier couple acide/base et une base d'un autre couple acide/base.
Dans ce chapitre on va introduire la notion d'équilibre chimique qui conduit vers un état d'équilibre. Cet équilibre chimique correspond à un avancement final de la réaction inférieur à l'avancement maximal observé dans le cas d'une réaction totale.
Complément :
L'atome d'hydrogène
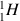 est composé d'un proton et d'un électron (il ne possède pas de neutron car le nombre de masse est égal au numéro atomique). Quand il perd son électron il devient l'ion
est composé d'un proton et d'un électron (il ne possède pas de neutron car le nombre de masse est égal au numéro atomique). Quand il perd son électron il devient l'ion
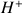 qui n'est donc plus constitué que d'un proton. D'où l'utilisation du terme proton pour désigner l'ion
qui n'est donc plus constitué que d'un proton. D'où l'utilisation du terme proton pour désigner l'ion
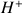 .
.
|