Indicateurs colorés
Définition :
Un indicateur coloré est constitué par un couple acide/base dont :
les réactions de dissociation de l'acide ou de la base dans l'eau ne sont pas totales. Tout comme tout couple acide/base, un indicateur coloré sera caractérisé par un
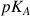 .
.
les espèces conjuguées (acide et base) ont des teintes différentes
- pour
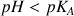 , l'indicateur coloré prendra la teinte de la forme acide
, l'indicateur coloré prendra la teinte de la forme acide
- pour
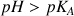 , l'indicateur coloré prendra la teinte de la forme basique
, l'indicateur coloré prendra la teinte de la forme basique
Une goutte d'indicateur coloré suffit pour colorer une solution.
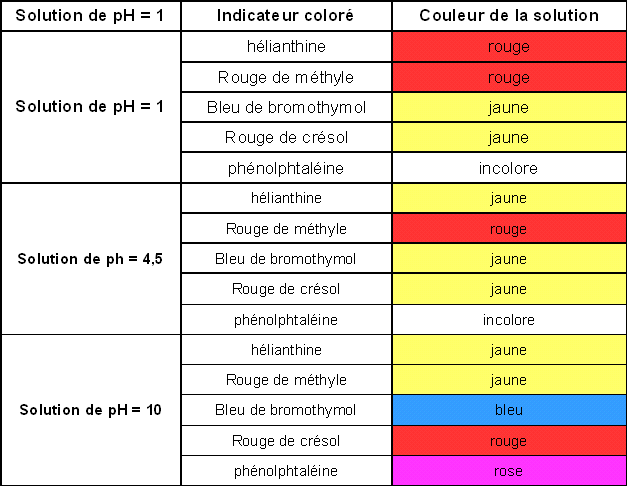
Voici une liste d'indicateurs colorés :
Exemple :
Remarque :
Il est évident que le changement de couleur n'est pas franc lorsque le pH de la solution est proche du
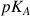 de l'indicateur coloré. Ainsi, une solution de pH = 7 contenant une goutte de bleu de bromothymol prendra une teinte verte (jaune + bleu). La zone de pH pour laquelle la couleur obtenue est un mélange des couleurs de la teinte acide et de la teinte basique est appelée zone de virage.
de l'indicateur coloré. Ainsi, une solution de pH = 7 contenant une goutte de bleu de bromothymol prendra une teinte verte (jaune + bleu). La zone de pH pour laquelle la couleur obtenue est un mélange des couleurs de la teinte acide et de la teinte basique est appelée zone de virage.