L'appareil photosynthétique dans le chloroplaste
Afin de déterminer la distribution et l'organisation de l'appareil photosynthétique dans le chloroplaste et en comprendre le fonctionnement, des études expérimentales ont été réalisées sur la structure du chloroplaste :
Les chloroplastes des plantes terrestres et des algues vertes, d'une taille de quelques micromètres généralement, sont limités par une enveloppe composée d'une membrane externe et d'une membrane interne.
Les chloroplastes sont des organites cellulaires comprenant plusieurs compartiments. Les membranes photosynthétiques forment des espèces de sacs aplatis dans le sens de la longueur du plaste. Les sacs peuvent être accolés entre eux, formant ainsi un granum (Figure 34). Ils contiennent tous les composés biochimiques nécessaires aux réactions photochimiques de la photosynthèse.
Les thylacoïdes baignent dans une matrice appelée stroma qui contient tous les composés biochimiques permettant d'assurer les réactions thermochimiques de la photosynthèse (Figure 34F) . Ce stroma peut également contenir :
un ou plusieurs grains d'amidon, de taille variable. La présence d'amidon témoigne de l'accumulation des produits du cycle de Calvin et représente une réserve énergétique mobilisable par la cellule végétale à tout moment (Figure 34B),
des globules lipidiques contenant notamment des caroténoïdes (Figure 34C) . Afin de les différencier des globules lipidiques cytoplasmiques, les globules lipidiques des plastes sont appelés plastoglobules,
de l'ADN, reliquat de la cyanobactérie à l'origine des plastes (endosymbiose). Il code pour une partie des protéines des plastes (ex: grande sous-unité de la RuBisCO). Associé à de l'ARN et des protéines, il forme des nucléoïdes (petites zones claires sans contour défini visibles en microscopie électronique à transmission),
des ribosomes 70S (typiques des procaryotes), lieux de synthèse des protéines codées dans le génome platidial,
des formes “cristallines” de phytoferritine. La ferritine est une protéine de mise en réserve du fer.
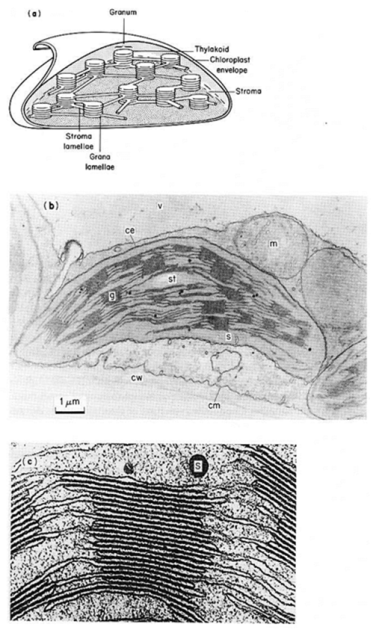
A. Vue schématique en 3D d'un chloroplaste. L'enveloppe, constituée d'une double membrane, est éclatée afin de permettre la visualisation du stroma. Celui-ci contient des empilements de thylacoïdes (thylakoïdes) formant un granum. Les grana sont connectés entre-eux par des lamelles stromales (en anglais “stroma lamellae”).
B. Coupe transversale d'une cellule chlorophyllienne observée au microscope électronique à transmission. Les deux membranes constituant l'enveloppe chloroplastique (ce) sont très visibles à certains endroits. Le stroma (s) contient de nombreux grana (g) et un grain d'amidon (st). Notez la présence de mitochondries (m) à proximité du chloroplaste.
C. La coupe transversale dans un empilement granaire observée au microscope électronique à transmission permet de visualiser l'empilement des thylacoïdes. L'intérieur de chaque thylacoïde est appelé lumière ou lumen. La photographie montre également un plastoglobule dense aux électrons (s).
Approche expérimentale
Comme nous venons de l'expliquer, les chloroplastes contiennent deux types de thylacoïdes à savoir les thylacoïdes non empilés reliant les grana et les thylacoïdes empilés formant les grana. Nous avons également vu que ces membranes contiennent l'appareil photosynthétique. Si les propriétés d'organisation des thylacoïdes sont différentes, qu'en est-il de leur contenu ? Pour répondre à cette question, isolons les deux types de thylacoïdes (Thylacoïde 1 = Thylacoïdes reliant les grana + zones de grana exposées au stroma des chloroplastes et Thylacoïde 2 = Thylacoïdes empilés formant le grana) pour en étudier le contenu en protéine.
Un protocole typique d'isolement des deux types de thylacoïdes est présenté dans la figure 35A. Il utilise des feuilles d'épinard dont les chloroplastes sont extraits dans du tampon. Les membranes photosynthétiques sont recueillies après un choc osmotique suffisamment intense pour briser les membranes entourant les chloroplastes et réparties en aliquots. Afin de libérer les protéines enchassées dans les thylacoïdes, les lipides des membranes sont solubilisés à l'aide d'un détergent (ex : Triton X-100). Noter que les détergents sont différents et utilisés dans des concentrations très différentes (faible concentration de détergent pour thylacoïde 1 et forte concentration pour thylacoïde 2). Les préparations sont ensuite centrifugées. Selon les traitements, c'est soit le surnageant soit le culot de centrifugation qui est conservé pour l'analyse protéique.
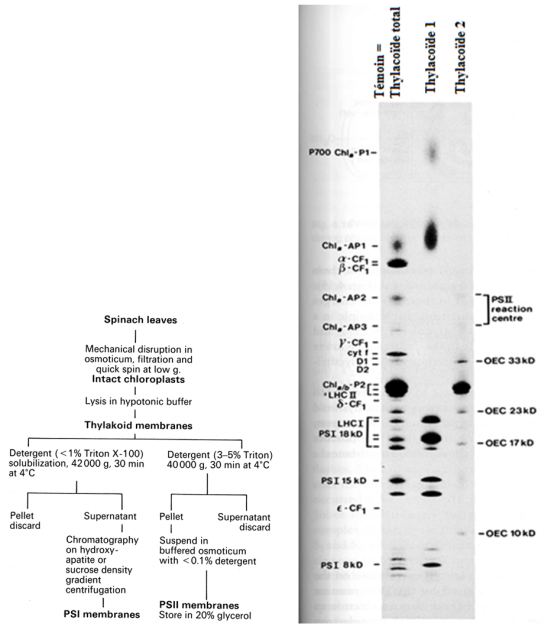
A. Protocole expérimental permettant la préparation des deux types de thylacoïdes. Il est important de noter que la concentration en détergent utilisée pour obtenir les deux types de thylacoïdes est très différente.
B. Comparaison des profils protéiques obtenus avec des fractions contenant les deux types de thylacoïdes « Témoin » (piste de gauche), la fraction « thylacoïde 1 » (piste médiane) et la fraction « thylacoïde 2 » (piste de droite). Les protéines sont identifiées par leur nom dans les zones bordant les pistes d'électrophorèse. La coloration des bandes de protéines a été réalisée au bleu de Coomassie.
Questions :
En comparant les bandes obtenues à partir de l'extrait « Témoin » et celles obtenues à partir des fractions « Thylacoïde 1 » et « Thylacoïde 2 », indiquez les bandes identifiées dans chacun des extraits, leur nombre : comment le justifiez-vous ?
L'ensemble des bandes obtenues à partir de l'extrait « Témoin » sont-elles présentes dans les fractions 1 et 2 ? Comment l'expliquez-vous ?
Des concentrations différentes de détergents ont dû être utilisées pour effectuer l'extraction des protéines membranaires au niveau des fractions 1 et 2 : quelle(s) interprétation(s) en donnez-vous ?
Réponses :
C'est dans la piste de l'extrait contenant les deux types de thylacoïdes (Témoin) que les bandes protéiques sont les plus nombreuses, ce qui est attendu. En revanche, l'extrait “thylacoïdes 1” n'a donné que 9 bandes : le complexe protéique le plus gros correspond aux centres réactionnels des PS I, puis viennent, par ordre décroissant de taille, le complexe apoprotéines-chlorophylles a et les protéines de l'antenne collectrice de l'énergie lumineuse associée au centre réactionnel du photosystème I (Fig. 34FB). Dans cette piste, aucune protéine appartenant au photosystème II n'est visible. Cette fraction est donc enrichie en photosystème I.
L'extrait “thylacoïdes 2” présente seulement 5 bandes bien visibles : la bande épaisse regroupe en fait plusieurs protéines de l'antenne collectrice du PS II, les autres bandes correspondent à des sous-unités du complexe permettant la production de dioxygène. Dans cette piste, aucune protéine appartenant au photosystème I n'est visible. Cette fraction est donc enrichie en photosystème II (Fig. 34FB).
Il est intéressant de noter que certaines protéines présentes dans l'extrait contenant les deux types thylacoïdes ne sont présentes dans aucune des deux autres pistes. Ceci signifie qu'elles ont été perdues lors de la préparation des deux fractions de thylacoïdes. Les protéines concernées appartiennent aux complexes cytochromes b6 et f et à l'ATP synthase.
Cette expérience démontre qu'en modifiant la concentration en détergent du tampon, il est possible d'isoler, soit les photosystèmes II, soit les photosystèmes I. Si l'on essaie de comprendre les raisons de ce résultat, le modèle présenté à la figure 35 suivant est obtenu. Il présente la distribution des photosystèmes I et II dans les membranes thylacoïdales. Nous avons constaté que lorsqu'une quantité faible de détergent est ajoutée à la préparation de thylacoïdes, une fraction enrichie en protéines typiques du photosystème I est obtenue. Cela signifie que les zones des thylacoïdes dans lesquels ce photosystème se trouve sont aisément accessibles aux molécules de détergent. Les photosystèmes I sont donc localisés dans les régions exposées au stroma du chloroplaste c'est à dire les membranes extérieures des empilements granaires et les thylacoïdes intergranaires. Au contraire, les protéines typiques du photosystème II ne sont obtenues que lorsque la concentration en détergent est élevée, indiquant que ces protéines sont localisées dans des endroits peu accessibles des thylacoïdes comme le coeur des empilements granaires. Dans le modèle, les photosystèmes II sont notés PSIIα. Ce modèle montre également que les complexes cytochromes b6f sont localisés dans les deux types de membranes alors que l'ATP synthase (noté dans la Fig. 35 comme CF0-CF1 complex) accompagne les photosystèmes I. La figure présente également la localisation des PSIIβ. Cette notation désigne des photosystèmes II n'émettant pas d'oxygène car leur antenne collectrice de l'énergie lumineuse et détachée des centres réactionnels (notées
« LHC2 mobile »
dans la Figure 35). Ces entités apparaissent en cas de stress. Nous en reparlerons à la fin de ce cours. Il est important de noter que ce modèle n'est valable que chez les plantes terrestres et les algues vertes.
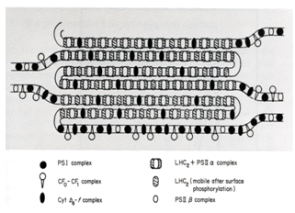
Les photosystèmes I et l'ATP synthase (CF0-CF1 complex) sont localisés dans les zones exposées au stroma du chloroplaste c'est à dire les membranes extérieures des empilements granaires et les thylacoïdes intergranaires tandis que les photosystèmes II sont dans les empilements granaires (PSIIα). Les complexes cytochromes b6f sont localisés dans les deux types de membranes. Les PSIIβ représentent des photosystèmes II n'émettant pas de dioxygène et des antennes collectrices de l'énergie lumineuse détachée des centres réactionnels qui se forment apparaissent en cas de stress.