Le Photosystème II
Apports scientifiques : nature, structure et fonction du photosystème II |
La figure 27 présente un schéma de l'organisation du photosystème II des plantes terrestres. Celui-ci est composé de protéines et de complexes protéines-pigments. Seuls les composés les plus importants sont décrits ici. Le centre réactionnel est composé du dimère formé des protéines-pigments D1 et D2. Au coeur du complexe est logée la paire spéciale de molécules de chlorophylle a dont nous avons parlé précédemment. Elle est appelée P680 car il s'agit d'un pigment absorbant à 680 nm. D1 et D2 partagent également un atome de fer (Fe) non hémique[1]. D1 et D2 lient chacun une molécule de phéophytine[2] (Pheo dans la figure 1.2.2.4.5.F1) et un type de quinone : la plastoquinone QB au niveau de D1 et la quinone QA au niveau de D2 (Figure 27). QA ne peut accepter qu'un seul électron à la fois tandis que QB peux en accepter deux.
Les complexes protéines-pigments CP43 et CP47 forment l'antenne collectrice interne de l'énergie lumineuse. La dénomination CP signifie « Chlorophyll Protein »
et le chiffre indique la masse moléculaire apparente de la protéine lorsqu'elle est séparée par gel d'électrophorèse SDS-PAGE[3]. Le polypeptide de 28 kDa représente l'antenne externe de l'énergie lumineuse. Le photosystème II contient d'autres protéines telles que le polypeptide I et le cytochrome b559 qui remplissent des rôles structuraux et dans le transfert des électrons autour du photosystème II. La description de ces rôles sort du cadre de cette ressource.
Comme l'illustre la figure 27, cet assemblage de protéines est disposé dans la membrane photosynthétique. Pour la compréhension du mécanisme, il est important de comprendre l'orientation des composants du photosystème II à savoir que les quinones se trouvent du côté exposé au lumen tandis que le P680 est situé du côté exposé au stroma. Du point de vue fonctionnel, l'énergie absorbée par l'antenne collectrice de l'énergie lumineuse arrive au niveau du P680 (flèche grise dans la figure 27) et provoque l'ionisation d'une des molécules de chlorophylle de ce dernier. P680 est relié électroniquement à la phéophytine a de D1. Dans la figure 27, les transferts d'électrons sont représentés par les flèches noires. Le transfert d'électrons vers la phéophytine a de D2 n'est jamais observé. L'électron ne reste que transitoirement au niveau de la phéophytine et est transféré à QA puis sur QB. Pour que QB soit saturé en électrons (QB2-), il faut donc que deux électrons aient quitté successivement P680. Ces électrons sont alors injectés dans la chaîne de transporteurs d'électrons, permettant à QB d'accepter de nouveaux électrons. Nous étudierons dans une section ultérieure les mécanismes sur lesquels repose ce transfert.
Quoiqu'il en soit, le vide électronique créé au niveau de P680 doit être comblé chaque fois qu'un électron est transféré à la phéophytine a. Le comblement du vide électronique rend la molécule de chlorophylle a à nouveau électriquement neutre et préserve sa stabilité. Si, au lieu de considérer chaque étape du mouvement des électrons de manière relativement statique comme nous venons de le faire, nous considérons le flux d'électrons, c'est à dire la dynamique du système, il devient rapidement évident que le transfert d'électrons à l'intérieur du photosystème II ne peut être performant que s'il existe une source d'électrons abondante et aisément mobilisable pour le comblement du vide électronique se créant régulièrement au niveau du P680. Cette source d'électrons est composée des molécules d'eau présentes dans la lumière des thylacoïdes (Beebo et al. 2013). Les polypeptides - EP33, EP17 et EP 24 - impliqués dans le système de photolyse de l'eau dont nous verrons le fonctionnement dans la prochaine section sont localisés dans le stroma des thylacoïdes. Le transfert de l'électron en provenance de l'eau vers le P680, s'effectue via un résidu histidine (YZ) du polypeptide D1.
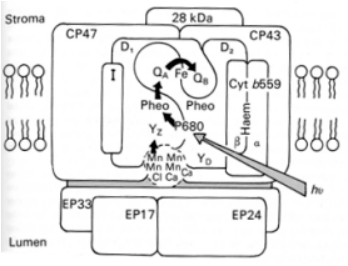
Le photosystème II est composé d'un centre réactionnel, le dimère D1 et D2, et d'une antenne collectrice de l'énergie lumineuse interne, CP43 et CP47, et externe, figurée par le polypeptide de 28 kDa. D'autres polypeptides tels que la protéine I et le cytochrome b559 sont également présents et remplissent des rôles structuraux et/ou de transfert d'électrons autour du photosystème II. Le centre réactionnel et les antennes collectrices sont disposés dans la membrane photosynthétique alors que les protéines impliquées dans la génération des électrons à partir des molécules d'eau sont localisées dans la lumière des thylacoïdes.
Du point de vue fonctionnel, l'énergie absorbée par l'antenne collectrice de l'énergie lumineuse arrive au niveau du P680 (flèche grise) et provoque la formation d'un cation de chlorophylle au niveau d'une des molécules de chlorophylle de ce dernier. L'électron généré est transféré (flèche noire) vers la phéophytine du polypeptide D1. L'électron ne reste que transitoirement à ce niveau et est transféré à QA puis à QB. Le vide électronique créé au niveau de P680 est comblé à l'aide d'un électron provenant de la photolyse de l'eau. Lors du transfert vers le P680, il passe par un résidu histidine (YZ) du polypeptide D1.
hν représente un quantum de lumière.
Hall and Rao (1994) Photosynthesis. 5th edition, Cambridge Univ Press, Fig 8.7, p163
Recherche de la source d'électrons : la photo-oxydation de l'eau |
Nous avons appris précédemment que lorsque l'énergie lumineuse collectée par l'antenne collectrice arrive au centre réactionnel, une des deux molécules de chlorophylle a de la paire spéciale du centre réactionnel perd un électron. Cette molécule se trouve sous forme d'un cation et est instable. Cet électron est injecté dans la chaîne de transporteurs. Le vide électronique ainsi créé doit être comblé par l'apport d'un électron, ce qui rétablit la neutralité électrique de la molécule donneuse. Nous avons également indiqué que ces électrons sont « extraits » de molécules d'eau présentes dans le stroma des thylacoïdes au cours d'un mécanisme appelé la photo-oxydation de l'eau en anglais. Nous allons maintenant découvrir comment ce mécanisme fonctionne. Deux groupes de chercheurs, l'un localisé en France (Joliot et al. 1969) et l'autre aux Etats-Unis d'Amérique (Kok et al. 1970), ont réalisé de manière indépendante, dans les années 1970, des expériences permettant d'élucider les bases de ce mécanisme. Dans cette expérience, des membranes photosynthétiques isolées sont placées à l'obscurité puis illuminées par un train d'éclairs de lumière de courte durée (10 µsec), les éclairs étant séparés les uns des autres par une courte période d'obscurité. Un résultat typique est présenté à la figure 28.
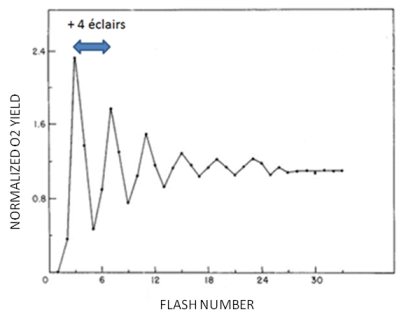
L'illumination de membranes photosynthétiques par un train d'éclairs de 10 µs, chacun séparé par une courte période d'obscurité ne donne pas lieu à une émission continue de l'oxygène. Celle-ci atteint un maximum tous les 4 éclairs. Ceci suggère que la photolyse d'une molécule d'eau requiert un mécanisme à 4 étapes. Le fait que le premier maximum soit observé lors du 3ème éclair suggère qu'à l'obscurité la molécule d'eau est déjà oxydée par un électron.
Questions :
Pourriez-vous caractériser l'allure de cette courbe d'émission d'oxygène ? Indiquez avec quelle fréquence d'éclairement les maximums sont atteints ? Que cela suggère-t-il ?
Réponses :
L'illumination de membranes photosynthétiques par un train d'éclairs de 10 µs, chacun séparé par une courte période d'obscurité ne donne pas lieu à une émission continue de l'oxygène. Celle-ci atteint un maximum tous les 4 éclairs. Ceci suggère que la photolyse d'une molécule d'eau requiert un mécanisme à 4 étapes. Le fait que le premier maximum soit observé lors du 3ème éclair suggère qu'à l'obscurité la molécule d'eau est déjà oxydée par un électron.
Il est aisé d'observer que la quantité de dioxygène émis à l'occasion de chaque éclair n'est pas constante mais qu'elle présente une oscillation de périodicité 4. KOK propose que l'émission de dioxygène passe par plusieurs états, qu'il appelle S (état = state dans la langue anglaise). Il y aurait donc 5 états S, S0-S4, chacun différent de l'autre par son état d'oxydation, ce dernier reflétant le nombre d'électrons extraits d'une molécule d'eau à l'occasion d'un éclair. Une représentation schématique de la réaction, placée dans son contexte biologique, est présentée dans la figure 29. Le système de dégagement de l'oxygène est localisé dans la lumière (ou lumen) des membranes thylacoïdales. La prise en charge des molécules d'eau permet la formation de l'état S0. Lorsqu'un éclair est absorbé, un premier électron est extrait. Afin de conserver la neutralité électrique un proton est également rejeté dans la lumière des thylacoïdes. C'est l'état S1. Le deuxième électron est extrait lors du deuxième éclair, générant l'état S2.Le troisième éclair provoque l'extraction d'un troisième électron et d'un deuxième proton. C'est l'état S3. Le quatrième éclair permet l'extraction du quatrième électron et la libération des deux protons restant, formant l'état S4. Ce dernier est très instable. La libération de la molécule d'oxygène régénère l'état S0 qui peut lier deux nouvelles molécules d'eau. Chaque électron est utilisé pour combler le vide électronique créé par l'ionisation d'une des deux molécules de chlorophylle du P680. Les protons sont déversés dans la lumière des thylacoïdes qui, en conséquence, s'acidifie (Figure 29). Le mécanisme de la photo-oxydation ne fonctionne qu'en présence de manganèse, de chlore et de calcium. Ces éléments sont indispensables pour l'extraction des électrons de la molécule d'eau.
Vous n'aurez pas manqué de remarquer que le premier maximum d'émission d'oxygène apparaît lors du 3ème éclair et que dans le cas précis de l'illumination d'un échantillon placé à l'obscurité, la périodicité de 4 ne s'installe pas immédiatement. Pour expliquer ce résultat, il faut admettre qu'au cours de la période d'obscurité qui précède la salve d'éclairs, l'état S1 est formé, ce qui suggère que les molécules d'eau ont déjà perdu un électron et un proton.
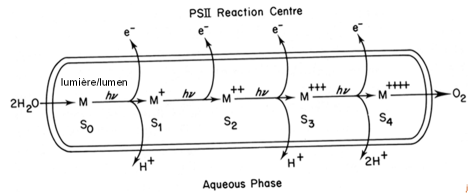
Les molécules d'eau présentes dans la lumière des membranes photosynthétiques entrent en contact avec le système de dégagement de l'oxygène localisé dans ce compartiment. La prise en charge des molécules d'eau permet la formation de l'état S0. Lorsqu'un éclair est absorbé, un premier électron est extrait. Afin de conserver la neutralité électrique, un proton est également rejeté dans la lumière des thylacoïdes. C'est l'état S1. Le deuxième électron est extrait lors du deuxième éclair, générant l'état S2. Le troisième éclair provoque l'extraction d'un troisième électron et d'un deuxième proton. C'est l'état S3. Le quatrième éclair permet l'extraction du quatrième électron et la libération des deux protons restants, formant l'état S4. Ce dernier est instable. La libération de la molécule d'oxygène régénère l'état S0 qui peut lier deux nouvelles molécules d'eau.