Le sarcomère comme unité de contraction
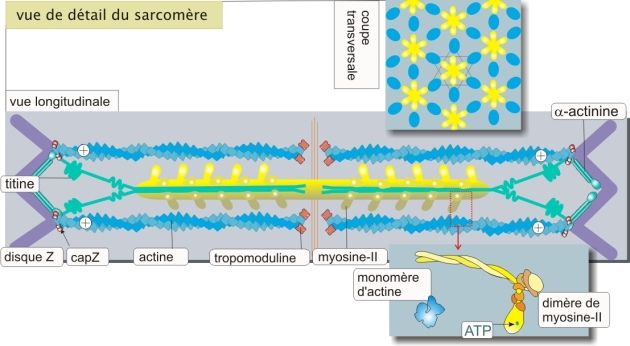
L'actine et la myosine sont à la base de la contractilité des sarcomères qui sont constitués par un assemblage de filaments parallèles d'actine (filaments minces) et de myosine-II (filaments épais) (figure 11 ci-dessous). Les filaments d'actine, longs d'environ 1\(\mu m\), sont attachés aux disques Z par l'intermédiaire de capZ (protéine de coiffage qui se fixe à l'extrémité plus) et de l'\(\alpha\)-actinine. L'extrémité moins (libre) est stabilisée par la tropomoduline. Sur sa longueur, le filament d'actine est associé à d'autres protéines qui interviennent dans la contraction musculaire (voir ci-dessous).
Les filaments de myosine-II, structures bipolaires résultant de l'association de nombreuses molécules de myosine-II, alternent régulièrement avec les filaments actine (figure 11 ci-dessus). La myosine-II est une protéine motrice formée d'une tête et d'une queue. La queue sert à insérer la protéine dans le filament et la tête, responsable d'une activité ATPase, interagit avec les filaments d'actine. Deux petites chaînes protéiques légères (17 kDa) entourent la myosine-II au niveau de la transition tête-queue.
Le filament épais de myosine-II est maintenu en place par un troisième filament, constitué de titine. C'est une protéine élastique d'environ 4000 kDa (~4MDa) (sa taille a valu son nom qui fait référence aux Titans, les divinités primordiales géantes qui ont précédé les Dieux de l'Olympe dans la mythologie grecque). C'est une des plus grandes protéines codées par le génome humain. La titine fait la liaison entre le disque Z et le filament épais de myosine-II. Par sa forme, la titine est une molécule élastique qui permet d'entretenir dans le muscle le phénomène de tension passive. De plus elle permet de centrer parfaitement le filament épais de myosine-II entre les filaments d'actine (figure 11 ci-dessus).
![]() Pour plus d'information sur la composition du disque-Z de sarcomère et sa liaison avec Titine, consultez le document suivant : « Titine structure Wilmanns [pdf] » (387 Ko)
Pour plus d'information sur la composition du disque-Z de sarcomère et sa liaison avec Titine, consultez le document suivant : « Titine structure Wilmanns [pdf] » (387 Ko)
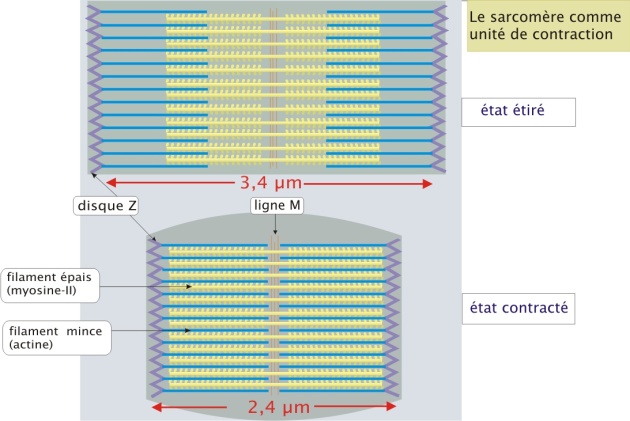
Le raccourcissement du sarcomère est provoqué par le glissement des filaments d'actine sur les filaments de myosine-II (force motrice), déclenché par l'hydrolyse de l'ATP (figure 12 ci-dessous).
Remarque : Remarques étymologiques
Sarco, du grec muscle, équivaut au latin myo. Le vocabulaire utilise indifféremment la racine grecque ou la racine latine. Par exemple on parle de myofibrilles, assemblage de sarcomères, contenant des filaments de myosine-II. Les myofibrilles sont entourées par du sarcoplasme (cytoplasme), contenant du réticulum sarcoplasmique (réticulum endoplasmique lisse), le tout emballé dans un sarcolemme (plasmolemme ou membrane plasmique).
![]() Pour en savoir plus, consultez le document suivant : « Titin Review Trinick [pdf] » (1350 Ko).
Pour en savoir plus, consultez le document suivant : « Titin Review Trinick [pdf] » (1350 Ko).