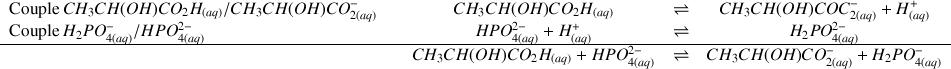Réactions acido-basique totale, avancement
On va étudier la réaction entre l'acide lactique
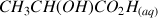 et l'ion hydrogénophosphate
et l'ion hydrogénophosphate
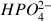 . Cette réaction est totale.
. Cette réaction est totale.
Question
a) Écrire la réaction acido-basique attendue entre d'acide lactique
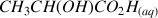 et l'ion hydrogénophosphate
et l'ion hydrogénophosphate
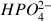 . Quels sont les couples acide/base mis en jeu ?
. Quels sont les couples acide/base mis en jeu ?
Question
b) On mélange 10 mL d'une solution d'acide lactique
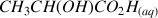 de concentration 0,20
de concentration 0,20
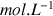 avec 15 mL d'une solution d'hydrogénophosphate de sodium (
avec 15 mL d'une solution d'hydrogénophosphate de sodium (
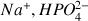 ) de concentration 0,15
) de concentration 0,15
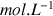 .
.
Établir le tableau d'avancement. Quelle est la valeur de l'avancement final et quels sont les quantités de matière des espèces en solution à la fin de la réaction ?
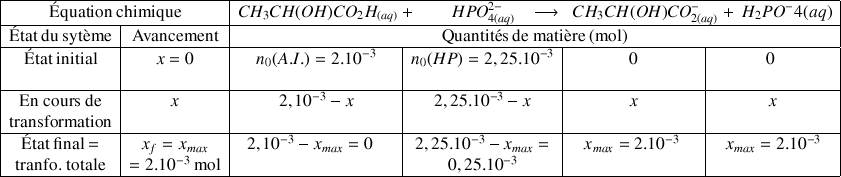
Nombre initial de mole d'acide lactique
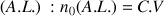
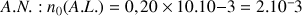 mol
mol
Nombre initial de mole d'hydrogénophosphate
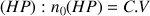
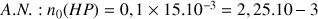 mol
mol
La réaction est totale donc on recherche le réactif limitant. On calcule les valeurs d'avancement maximal en considérant que chacun des réactifs est consommé
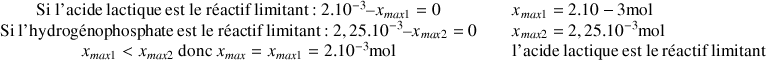
D'après le tableau d'avancement à la fin de la réaction il reste 0 mole de
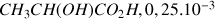 mol de
mol de
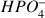 et il est apparu 2.10-3 mol de
et il est apparu 2.10-3 mol de
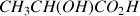 ,
,
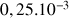 mol de
mol de
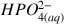 et il est apparu
et il est apparu
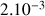 mol de
mol de
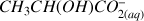 et
et
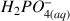 .
.