Deuxième GTPase : Rab1 et son rôle dans le recrutement des protéines accessoires de fusion
Rab1 (« Rat brain1 ») s'insère dans la membrane du REr au niveau d'un « site de sortie » par deux chaînes géranylgéranyl ( pour plus de détail sur la structure de Rab5 et sa liaison avec la membrane). Après le chargement en GTP, par RabGEF, Rab1 recrute les golgines (p115, GM130 et giantine, protéines d'arrimage de 50 nm de longeur) et l'ATPase NSF (voir figure 19). Comme cela a déjà été précisé plus haut, ces protéines sont indispensables dans la biogenèse du Golgi, mais leur rôle exact n'est pas encore connu Cependant, pour NSF on sait qu'il joue un rôle essentiel dans le démantèlement du complexe Q– et R–SNAREs sur la même membrane (« conformation-cis »). Le recrutement de p115 conduit à l'attachement au site de sortie d'autre protéines, telles que l'enzyme phospholipase–C\(\gamma\)1 et phospholipase D (qui changent la composition lipidique de la membrane de la vésicule bourgeonnante) et le facteur d'échange d'Arf1, GBF1 (Golgi-specific Breveldin–A–resistant factor).
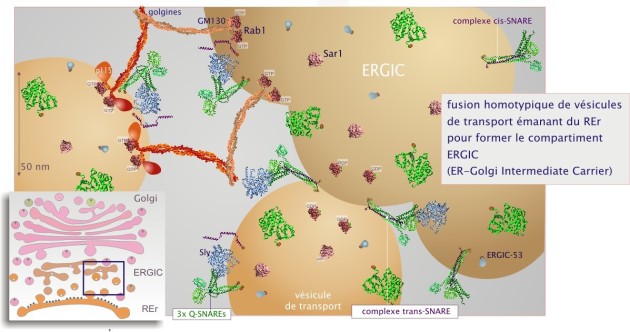
Les structures vésiculaires (et tubulaires) ainsi mises en place, et chargées des protéines destinées au Golgi, vont ensuite se séparer du REr (fission). Presque simultanément, le GTP de Sar est hydrolysé et le manteau COPII se disloque (sans perte de la machinerie de fusion). Les vésicules alors libérées (60-90 nm de diamètre environ) fusionnent entre elles, fusion homotypique, par un processus dirigé par Rab1, p115 et les SNAREs. Ensemble, elles donnent naissance à des cavités irrégulières (d'une taille d'environ 0,4-1,0 \(\mu \rm m\)) formant le compartiment ERGIC (ER Golgi intermediate carrier) (voir figure 20).
Remarque : Golgines
Les golgines furent à l'origine identifiées comme un groupe d'antigènes de poids moléculaire variable (p115, p130, etc.), à localisation golgienne, reconnues par des antisérums (anticorps) provenant de patients souffrant de maladies auto-immunes variées.
Elles ont en commun de longues séquences d'acides aminés, connues pour former des structures en torsade (« coiled-coil »), créant ainsi des complexes protéiques en forme de bâtonnet (jusqu'à 50 nm de longueur, c'est-à-dire d'une dimension comparable à celle de la vésicule qui les portent). Les golgines sont en général des protéines cytoplasmiques solubles recrutées à la membrane par fixation aux GTPases de la famille Rab (dans leur état lié au GTP). Elles sont indispensables aux évènements d'arrimage précédant la fusion vésiculaire et, grâce à leurs interactions avec la tubuline, elles interviennent dans l'organisation structurale du Golgi.
![]() Pour en savoir plus, consultez les documents suivants : « Golgins, Barr » [pdf] (475 Ko), et « SNARE, rSly, Hay » [pdf] (700 Ko).
Pour en savoir plus, consultez les documents suivants : « Golgins, Barr » [pdf] (475 Ko), et « SNARE, rSly, Hay » [pdf] (700 Ko).