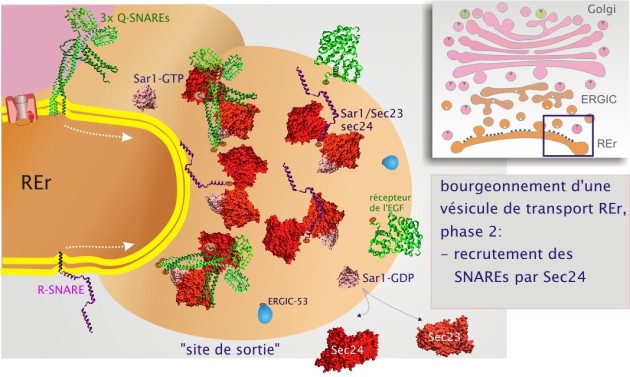
Première GTPase : Sar1 et son rôle dans le recrutement des protéines du manteau et de la charge
La GTPase Sar1 (« secretion associated ras-superfamily gene1 »), toujours liée à la membrane, est chargée de GTP par le facteur d'échange (GEF) Sec12p. Dans son état liant le GTP elle initie le tri de charge, en concentrant certaines protéines dans le domaine membranaire appelé « site de sortie » (qui forme progressivement un tube ou une vésicule, voir figure 17). Sar1–GTP recrute deux grands complexes, Sec23/24p et Sec13/31p. Leur attachement à la membrane et leur regroupement engendre la formation du manteau de type COPII. Cette charpente amorce la courbure de la membrane du REr, premier stade dans la formation du bourgeon.
i pour plus de détail sur le complexe Sar1 et Sec23/24.
pour plus de détail sur le récepteur de l'EGF lié à Sec24.
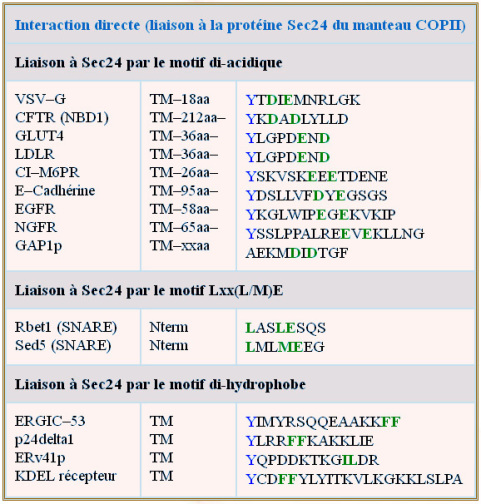
La protéine Sec24 joue un rôle important dans la fixation de la charge. Elle fixe des récepteurs transmembranaires qui contiennent un domaine diacidique, acide aspartique (D) et acide glutamique (E) dans des combinaisons DxD, DxE, ExD ou ExE, (en aval d'un résidu tyrosine clé) (cliquez sur les loupes sous la figure 17 pour plus de détails). Plusieurs isoformes de Sec24 existent, chacune pouvant avoir une affinité différente pour la charge. La charge soluble est aussi reconnue par des récepteurs transmembranaires, à leur tour reconnus par des protéines du manteau. Par exemple, des glycoprotéines telles que la cathepsine Z et les facteurs de coagulation V et VIII, sont capturés par le récepteur-lectine ERGIC–53, lui-même reconnu par Sec24 par son motif dihydrophobe C–terminal (AKKFF–COOH). La protéine disulfure isomérase (PDI) et la chaperonne BiP sont capturées par une protéine transmembranaire qui fixe leur séquence lys–asp–glu–leu–COOH (KDEL), pour cela appelée récepteur KDEL (protéine 6 fois transmembranaire et d'un poids moléculaire de 37 kDa). Comme on le verra plus tard, le motif KDEL détermine aussi le transport rétrograde (du Golgi au REr).
Ensuite, Sec24 joue également un rôle important dans le recrutement de la machinerie de fusion : les Q–SNAREs, Syntaxine–5 (sed5), Sec22B et Membrine (Bos1) ; le R–SNARE, rBet1. La SM protéine rSly rejoint également les protéines de fusion (voir figure 18).
pour plus de détail sur la fixation des SNAREs par Sec24.
Le processus sélectif dépendant d'un récepteur, qui vient d'être décrit, est probablement accompagné d'un transport en bloc, non-sélectif. En effet, au cours de leur bourgeonnement, les vésicules peuvent capturer accidentellement des protéines solubles. Si les protéines sont indésirables, elles sont alors soumises à un transport rétrograde, qui les renvoie vers le REr, dans des vésicules du type COPI (voir plus tard).
Le manque de l'activité Sar1p, dû à une mutation de la thréonine en position 39 (remplacée par l'asparagine, T39N) qui empêche l'échange de GDP par GTP, cause une complète dislocation de l'appareil de Golgi, démontrant ainsi la place unique du REr dans la biogenèse du Golgi.
Peptides de destination pour quitter le REr

Remarque :
La protéine ERGIC–53, est un récepteur-lectine (d'un poids de 53 kDa), dépendant du Ca2+, à forte affinité pour le mannose et dont le nom est dû au fait qu'elle est particulièrement présente dans le compartiment intermédiaire ERGIC. L'ERGIC–53 est une protéine transmembranaire type 1 (C–terminal du coté cytoplasmique).
![]() Pour en savoir plus, consultez les documents suivants : « COPII cargo selection overview » [pdf] (80 Ko), et « COPII Sec23-24-Sar1 structure » [pdf] (713 Ko).
Pour en savoir plus, consultez les documents suivants : « COPII cargo selection overview » [pdf] (80 Ko), et « COPII Sec23-24-Sar1 structure » [pdf] (713 Ko).