1. Généralités
Dans ce chapitre, nous évoquons les approches qui partent du principe que les propriétés recherchées sont entièrement encodées dans la structure chimique du composé d'intérêt. Le défi est alors de trouver une métrique qui permet de décoder et de quantifier la propriété recherchée. On tente donc d'établir des relations quantitative entre des structures chimique et des propriétés (ici de nature pharmacologiques). On parle d'approche QSAR, pour Quantitative Structure-Activity Relationship. Nous allons nous focaliser sur l'approche dite pharmacophore.
Définition :
Un pharmacophore est l'ensemble des caractéristiques stériques et électroniques nécessaires pour assurer des interactions optimales avec une cible biologique et déclencher ou inhiber sa réponse.
De manière plus pragmatique, il s'agit des caractéristiques chimiques et physico-chimiques que devra posséder une molécule pour interagir de manière optimale avec sa cible pharmacologique.
Exemple :
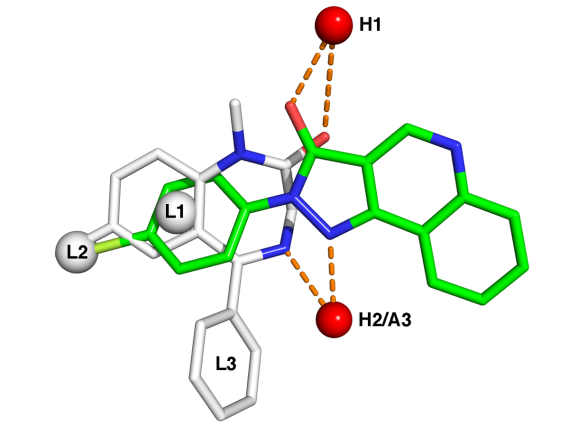
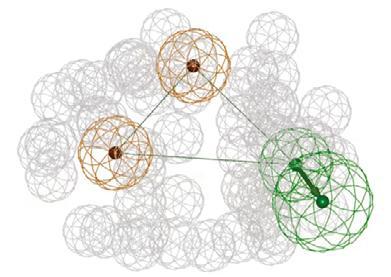
La figure représente la superposition de 2 molécules ayant des activités comparable sur un récepteur GABA. La molécule blanche représente le diazepam (benzodiazépine , aussi appelée valium) et la molécule verte représente la molécule CGS-9896 (non-benzodiazépine). Ces deux molécules n'appartiennent pas à la même famille chimique mais partagent le même pharmacophore. Le pharmacophore est représenté par des sphères, associées à des propriétés physico-chimiques disposées dans l'espace. Les sphères rouges sont des sites donneurs (H1) ou donneurs et accepteurs (H2/A3) de liaisons hydrogènes. Les sphères blanches sont des sites d'interaction non polaire (lipophile).
Attention :
Le pharmacophore n'est donc pas une molécule, c'est une représentation en 3 dimensions des caractéristiques nécessaires pour générer une effet biologique.
Ces caractéristiques sont typiquement :
des sites privilégiant des interactions directionnelles :
des site accepteurs de liaison hydrogène (par exemple : -O, -N)
des sites donneurs de liaison hydrogène (par exemple : -OH, -NH)
des sites donneurs/accepteurs de liaison hydrogène (par exemple : -COOH, -NH2)
des sites d'interaction non-directionnels :
des sites de contact hydrophobe (par exemple : -CH3)
des site chargés électriquement (par exemple : -NH3+, -COO-)
des cycles aromatiques
des zones d'exclusion, celles où il est préférable de ne pas avoir d'atome
Exemple :