4.3.1 Définition
Définition : Les dérivés halogénés
Les dérivés halogénés sont des espèces capables de réagir avec des entités possédant une paire d'électrons non liants (un anion ou une molécule neutre possédant un doublet libre, comme un atome d'azote par exemple) de façon à éliminer l'halogène en le remplaçant par cette nouvelle entité. C'est ce que l'on appelle une substitution nucléophile, il en existe de plusieurs sortes qui sont décrites ci-après.
En chimie organique, on note le nucléophile par l'abréviation 'Nu'. Un nucléophile est aussi une base de Lewis, c'est-à-dire une entité qui possède une paire libre d'électrons.
La réaction de substitution nécessite quelques explications quand au vocabulaire utilisé, on a vu que le nucléophile est l'espèce entrante. L'halogène qui va partir est quand à lui appelé nucléofuge ou plus simplement groupe partant (Leaving Group, pour les anglo-saxons). Les nucléophiles sont classés par "force" et il en va de même pour les groupes partant. Ainsi, pour qu'une réaction de substitution ait lieu dans les meilleures conditions, il faut un très bon groupe partant et un très bon nucléophile.
Pour qu'un groupe partant soit le meilleur possible, il faut que la liaison carbone-groupe partant soit la plus faible possible. Cette liaison est la plus faible pour X = I > Br > Cl > F (Plus l'halogène est gros et plus la liaison est faible).
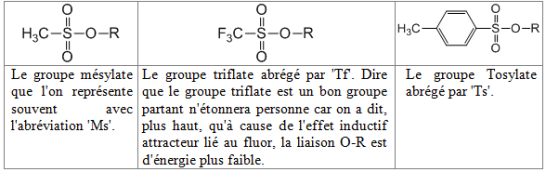
Les halogènes ne sont pas les seuls bons groupes partant, d'autres groupes tels que les mésylates, tosylates et autres sulfonates sont de très bons groupes partant :