4.1 Généralités
Les dérivés halogénés sont des composés qui possèdent une liaison carbone-halogène. L'halogène pouvant être le fluor, le chlore, le brome ou l'iode. Plus on descend dans la classification périodique et plus l'atome d'halogène est gros. Plus l'atome d'halogène est gros et plus la liaison carbone-halogène est faible et donc facile à rompre.
La liaison carbone-halogène est polarisée selon :
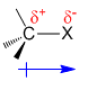 Fig. 1 | Il est à noter que de façon générale, en chimie organique, la lettre X représente un halogène quelconque à savoir le fluor, le chlore, le brome ou l'iode. |
Les composés bromés et chlorés sont largement utilisés pour préparer des magnésiens (voir le chapitres sur les organométalliques). Quand au fluor on l'utilise sous la forme du groupe -CF3 qui présente des propriétés électroniques particulières. En effet dans le cas de -CF3, on note un effet inductif attracteur particulièrement important.
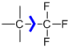 Fig. 2 | Conséquence pratique sur l'acidité : CF3SO3H est plus acide que son homologue CH3SO3H à cause de cet effet inductif attracteur. |





