Application à la datation : cas de la datation au carbone 14
Il existe deux isotopes stables du carbone dans la nature : le
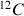 représentant 98,9% et le
représentant 98,9% et le
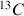 (1,1%). A ces isotopes s'ajoute entre autres le
(1,1%). A ces isotopes s'ajoute entre autres le
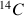 dont la période vaut 5730 ans. Il est beaucoup plus rare que les deux autres, son abondance par rapport au
dont la période vaut 5730 ans. Il est beaucoup plus rare que les deux autres, son abondance par rapport au
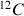 étant égale à
étant égale à
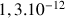 . Elle est constante car le « stock » de
. Elle est constante car le « stock » de
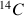 est constamment réapprovisionné par le bombardement du
est constamment réapprovisionné par le bombardement du
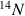 par les rayons cosmiques. Cette abondance relative est identique dans tous les êtres vivants (échanges de
par les rayons cosmiques. Cette abondance relative est identique dans tous les êtres vivants (échanges de
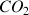 ). Quand l'organisme meurt, la quantité de
). Quand l'organisme meurt, la quantité de
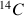 diminue par désintégration suite à l'arrêt des échanges avec le milieu extérieur.
diminue par désintégration suite à l'arrêt des échanges avec le milieu extérieur.
Si on connaît la quantité de carbone dans l'échantillon et l'activité à l'instant t, on peut donc déterminer la date de la mort de l'organisme. La datation au
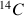 permet de dater des événements anciens de 40000 ans au maximum.
permet de dater des événements anciens de 40000 ans au maximum.
Pour des temps plus longs (en géologie par exemple), on utilise d'autres éléments radioactifs comme
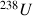 (période de 4,5 milliards d'années) ou le
(période de 4,5 milliards d'années) ou le
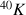 (
(
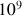 ou
ou
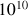 ans selon la réaction).
ans selon la réaction).






