Solution électrolytique
Définition : Solution électrolytique
Une solution électrolytique est une solution qui contient des ions. C'est la présence de ces espèces chargées (cations et anions) qui fait que cette solution conduit l'électricité.
On peut obtenir une solution électrolytique en dissolvant dans l'eau :
un solide ionique
NaCl(s) → Na+(aq) + Cl-(aq)
un liquide polaire
HNO3(l) → H+(aq) + NO3-(aq)
un gaz polaire
HCl(g) → H+(aq) + Cl-(aq)
Les liquides et les gaz polaires sont composés de molécules polaires qui vont se dissocier sous forme d'ions dans l'eau.
Rappel : Molécule polaire
Une liaison entre deux atomes A et B est dite polaire si les électrons de liaisons ne sont pas répartis équitablement entre ces deux atomes. L'atome plus électronégatif va plus attirer les électrons de liaison ce qui entraîne l'existence d'une charge partielle négative
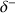 qui est compensée par une charge partielle positive
qui est compensée par une charge partielle positive
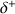 sur l'autre atome moins électronégatif. L'existence de cette différence de charge entraîne l'existence d'un moment dipolaire qui est une grandeur vectorielle qui a pour dimension le Coulomb.mètre (C.m). En chimie le vecteur moment dipolaire est orienté de l'atome qui porte la charge partielle positive vers l'atome qui porte la charge partielle négative (voir figure ci-dessous).
sur l'autre atome moins électronégatif. L'existence de cette différence de charge entraîne l'existence d'un moment dipolaire qui est une grandeur vectorielle qui a pour dimension le Coulomb.mètre (C.m). En chimie le vecteur moment dipolaire est orienté de l'atome qui porte la charge partielle positive vers l'atome qui porte la charge partielle négative (voir figure ci-dessous).
Une molécule est dite polaire si la somme vectorielle de moments dipolaires de toutes les liaisons polarisées de la molécule est non nulle. Autrement dit, une molécule est polaire si le barycentre des charges partielles négatives et le barycentre des charges partielles positives ne sont pas confondus.
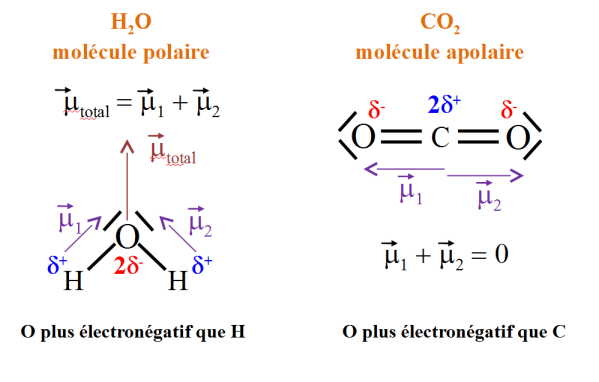
Exemple :
Les molécules H2O et CO2
On observe une polarisation des liaisons H-O et C-O car les atomes d'oxygène sont beaucoup plus électronégatifs (attracteurs d'électrons) que les atomes de H et de C.
Dans le cas de la molécule H2O la somme des vecteurs correspondant aux moments dipolaires
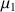 et
et
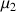 des liaisons H-O donne un vecteur correspondant au moment dipolaire total
des liaisons H-O donne un vecteur correspondant au moment dipolaire total
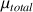 La somme des vecteurs n'étant pas nulle, l'eau est une molécule polaire.
La somme des vecteurs n'étant pas nulle, l'eau est une molécule polaire.
Dans le cas de la molécule CO2, la somme des vecteurs correspondant aux moments dipolaires
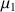 et
et
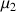 des liaisons C-O est nulle, le dioxyde de carbone est donc une molécule apolaire.
des liaisons C-O est nulle, le dioxyde de carbone est donc une molécule apolaire.