Les chaînes de glycosaminoglycanes (GAG)
Les chaînes de glycosaminoglycanes (GAG)
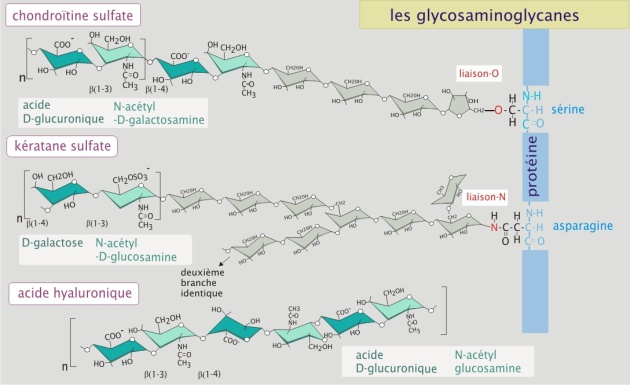
Les glycosaminoglycanes sont de longues chaînes composées d'unités disaccharidiques répétitives. Un des deux résidus glucidiques est toujours un glucide aminé (N-acétylglucosamine ou N-acétylgalactosamine) et le second est habituellement un acide uronique (glucuronique ou iduronique). Les GAG se répartissent en quatre types principaux :
l'acide hyaluronique (d'hyaloïde (humeur vitrée) et acide uronique),
la chondroïtine sulfate,
l'héparane sulfate et
le kératane sulfate.
A l'exception de l'acide hyaluronique, tous les GAG sont liés de façon covalente à une protéine pour former des protéoglycanes (trois exemples de GAG sont présentés dans la figure 14).
Cliquez pour plus de détail
Les GAG, particulièrement l'acide hyaluronique, forment des mailles qui leur permettent d'absorber de grandes quantités d'eau (grâce à leur charge). Ils constituent un gel d'un volume considérable, 1 000-10 000 fois le volume initial. Cela crée une pression de gonflement, ou turgescence, qui permet à la matrice de résister aux forces de compression. Dans le cas de l'acide hyaluronique, les chaînes de plus de 50 000 répétitions peuvent exister, atteignant une longueur de 4 mm.
Exemple : Quelques exemples illustrent la contribution des GAG aux fonctions de la matrice extracellulaire
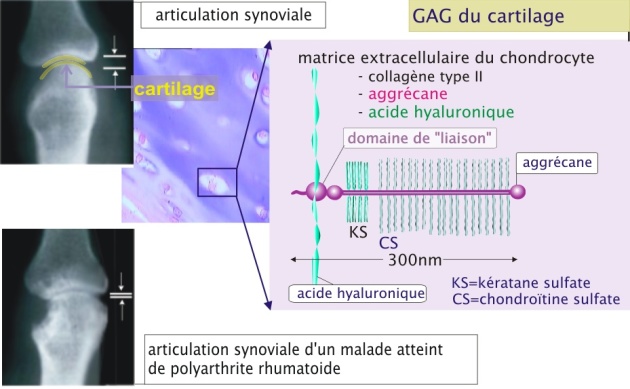
Le cartilage hyalin contient de l'acide hyaluronique, de la chondroïtine sulfate et du kératane sulfate (ces deux derniers associés avec un noyau de protéines pour former l'aggrécane (poids moléculaire d'environ 250 kDa). L'aggrécane et un autre composant protéique du cartilage (protéine de liaison du cartilage) contiennent un domaine qui permet l'interaction avec l'acide hyaluronique. Les deux (protéine et GAG) constituent un formidable « absorbeur de chocs ». Dans la polyarthrite rhumatoïde, l'état inflammatoire chronique résulte en une perte de cartilage accompagnée d'une érosion de l'os avec pour résultat un mauvais fonctionnement de l'articulation. La radiographie en figure 15 montre que les deux os se rapprochent suite à la perte de cartilage (ligne jaune).
Autres exemples :
La crête du coq et le placenta dont la turgescence est permise grâce à la présence de quantités importantes d'acide hyaluronique.
Les GAG ont aussi un rôle essentiel dans la migration cellulaire au cours de la morphogenèse et de la cicatrisation des tissus (voir aussi le paragraphe sur la protéine de liaison du cartilage). En cas de blessure, après la coagulation du sang, le premier produit qui entre dans la lésion est l'acide hyaluronique. Il forme un échafaudage qui va servir de support aux cellules leucocytaires et aux fibroblastes pour reconstruire le nouveau tissu.