Ep. 11 - Utilisations des mycètes
Quand on aborde les bienfaits des mycètes pour l'Homme, on pense généralement en premier lieu aux bénéfices alimentaires provenant des espèces comestibles. Il ne faut pas oublier non plus l'énorme contribution des champignons à l'élaboration de produits pharmaceutiques et à la biotechnologie. D'ailleurs, l'utilisation des champignons pour la production de vin et de pain levé marque sans doute le point à partir duquel les humains ont appris à manipuler le monde naturel pour effectuer des réactions chimiques bénéfiques. Cette histoire se poursuit actuellement en considérant les cellules fongiques comme des usines capables de produire des composés chimiques précieux, ce qui constitue le fondement de la biotechnologie moderne.
Globalement, les mycètes présentent plusieurs avantages pour la production industrielle :
- leur génome est assez facilement manipulable ;
- en tant qu'osmotrophes, ils ont un appareil de production et de sécrétion des protéines et d'autres métabolites très performant (les rendements de production sont très au-dessus de ce qu'on peut obtenir avec d'autres organismes) ;
- les mycètes choisis pour ces approches sont facilement cultivables à très grande échelle permettant d’accroître les rendements de production.
Les mycètes comestibles (ou non ... )
Au moins 350 espèces fongiques sont consommées en tant qu'aliments. Ces espèces comestibles proviennent de seulement 18 ordres de champignons, ce qui représente une petite fraction de la diversité fongique totale. Les espèces les plus couramment consommées et commercialisées sont les Russules (Russula spp.), les lactaires (Lactarius spp.), les chanterelles (Cantharellus spp.), les agarics (Agaricus spp.) et les bolets (Boletus spp.). La plupart des espèces sauvages récoltées classiquement dans la nature ne peuvent être cultivées en raison de dépendances nutritionnelles complexes. La dizaine d'espèces cultivables a été sélectionnée pour leur capacité à se nourrir de matières organiques mortes, ce qui les rend plus faciles à cultiver en grandes quantités. La plupart sont des Basidiomycètes dont la partie comestible est constituée par le carpophore : champignon de Paris, Pleurotes (Pleurotus ostreatus), Shi-take (Lentinus edodes).
https://www.flickr.com/photos/125349922@N05/14373056430/in/photostream/
https://www.flickr.com/photos/125349922@N05/14536216556/in/photostream/
https://www.flickr.com/photos/125349922@N05/14536288196/in/photostream/
Néanmoins, il est nécessaire de bien identifier les champignons que l'on souhaite cuisiner. 8 000-10 000 cas d'empoisonnements sont recensés en France par an. Dans la plupart des cas, les conséquences sont heureusement bénignes et se traduisent par des syndromes gastro-intestinaux à latence courte qui apparaissent généralement entre 30 min et 1h30 après ingestion. Dans les cas les plus sévères, la période de latence est plus longue, les premiers symptômes mettant au moins 6h à apparaître. Les responsables de ces affections sévères sont une petite dizaine regroupée principalement au sein de 3 genres : Amanita, Gyromitra, Cortinarius et synthétisent des toxines à l'origine des symptômes. Le genre Amanita est responsable à lui seul de plus de 90% des empoisonnements mortels recensés en France. Dans la majorité des cas, l'espèce incriminée est l'amanite phalloïde qui produit, l'alpha-amanitine, une toxine puissante de nature peptidique qui bloque l'expression des gènes. Les premiers symptômes du syndrome phalloïdien commence par des troubles digestifs violents généralement 12h après ingestion. Les cellules du foie sont ensuite attaquées et va conduire à une étape ultime au cours de laquelle le foie, les reins, le pancréas et les intestins cessent de fonctionner. Des troubles cérébraux peuvent apparaître suivis par un coma et le décès. Seuls des traitements très lourds, consistant en des dialyses et des greffes ont permis de réduire le taux de mortalité.
D'autres champignons, dits hallucinogènes, sont consommés depuis la nuit des temps pour modifier les états de consciences dans le cadre de cérémonies religieuses ou à titre récréatif. Différentes espèces ont des propriétés hallucinogènes, notamment dans les genres Psilocybe et Conocybe, qui contiennent deux puissantes substances hallucinogènes : la psilocybine et la psilocine.

https://commons.wikimedia.org/wiki/File:Amanita_phalloides_98857212.jpg
https://commons.wikimedia.org/wiki/File:Psilocybe_semilanceata.jpg
Productions et transformations alimentaires
Les champignons jouent également un rôle essentiel dans la production de denrées alimentaires et de boissons. Les levures alimentaires sont par exemple utilisées en tant qu'ingrédient culinaire dans l'alimentation animale ou humaine sous forme de paillettes. Elles sont particulièrement riches en protéines et en vitamines. Les extraits de levures sont aussi des ingrédients clé de certaines pâtes à tartiner. Des mycoprotéines sont aussi des ingrédients dans certaines préparations substituts de viande.
Certains mycètes sont par ailleurs d'excellents outils de biotransformation des aliments, notamment ceux qui sont capables de vivre sans respirer mais en utilisant le processus de fermentation. Par exemple, certaines levures vont transformer des sucres comme le glucose ou le fructose en éthanol et dioxyde de carbone via la fermentation alcoolique. Cette capacité est utilisée pour la fabrication du pain pour aérer la pâte (grâce au CO2) et des boissons alcoolisées. Les champignons sont également indispensables à la production de certains types de fromages, avec des moisissures telles que le Penicillium camemberti et P. roqueforti utilisé pour affiner et donner du goût au fromage.
Médicaments fongiques
Les champignons sont aussi sources de contributions non négligeables pour le monde de la médecine. Avant l'avènement de l'industrie pharmaceutique et des synthèses chimiques en laboratoire, la pharmacopée traditionnelle était issue de la nature et notamment des champignons. On peut rappeler ici un exemple marquant de cette pharmacopée d'origine fongique : « le champignon-chenille », Ophiocordyceps sinensis, parasite d'insecte qui se développe sur les larves de lépidoptères et qui entrent dans la composition de remèdes contre diverses pathologies (fatigue, maladies cardiaques, troubles rénaux, cancers...) en chine.
Pour la médecine plus contemporaine, les contributions médicales des mycètes sont nombreuses. Divers métabolites fongiques ont été utilisés ou ont été copiés pour intégrer des médicaments. Ils sont destinés à divers usages thérapeutiques : par exemple des antibiotiques pour lutter contre les infections, des immunosuppresseurs pour prévenir le rejet des greffes ou pour traiter la sclérose en plaques, des régulateurs du métabolisme lipidique pour diminuer les taux de cholestérol, ou encore des anti-migraineux.
En médecine contemporaine, l'élément le plus marquant est sans aucun doute la découverte du premier antibiotique, la pénicilline, par Alexander Fleming en 1928.
En outre, on a découvert que plusieurs médicaments de chimiothérapie, ou leurs précurseurs naturels, qui étaient à l'origine isolés des plantes, sont non seulement synthétisés par les cellules végétales mais synthétisés par des champignons endophytes vivant à l'intérieur de ces plantes. Le taxol ou paclitaxel en est un exemple : il a été découvert à l'origine comme un composé chimique synthétisé par l'if du Pacifique (Taxus brevifolia), mais il a depuis été signalé qu'il était synthétisé indépendamment par deux espèces fongiques différentes, Taxomyces andreanae et Penicillium raistrickii, qui vivent à l'intérieur de l'if.
Outre les composés chimiques produits naturellement par les champignons, les levures génétiquement modifiées jouent également un rôle important en médecine - en tant qu'usines vivantes pour la production de médicaments à base de protéines tels que les vaccins et les protéines thérapeutiques humaines. La capacité des espèces de levure telles que Saccharomyces cerevisiae et Komagataella pastoris (anciennement connu sous le nom de Pichia pastoris) pour produire efficacement des protéines humaines, fait que 15% des produits biopharmaceutiques sont maintenant produites à l'aide de cellules de levure. L'insuline et le vaccin contre l'hépatite B en sont des exemples notables.
Production d'enzymes et autres métabolites
Les enzymes sont des molécules naturelles qui catalysent des réactions chimiques. Elles sont particulièrement utilisées dans l'industrie, car elles façonnent les processus chimiques industriels. Les processus industriels qui nécessiteraient normalement des températures élevées ou des produits chimiques agressifs peuvent être réalisés dans des conditions beaucoup plus douces en utilisant des enzymes et les champignons se sont avérés une source utile : 60% des enzymes utilisées dans l'industrie proviennent de champignons et 70% d'entre elles sont dérivées de seulement sept espèces de champignons.
À titre d'exemples, des enzymes fongiques de type cellulase et laccase sont utilisées pour la fabrication du papier, processus pendant lequel le bois doit être décomposé en une pâte souple ;
des lipases issues d'Aspergillus intègrent des lessives ou des détergents ; des amylases et invertases permettent de modifier des sucres et sont utilisées en confiserie et dans la fabrication de jus et de sirop, tout comme les pectinases qui servent à clarifier les jus de fruit.
Les mycètes produisent d'autres types de métabolites qui peuvent être utilisés comme des additifs alimentaires (des arômes, des conservateurs, des vitamines ou précurseurs de vitamines), des agents de formulation, ou comme intrants agricoles (de composés jouant le rôle d'hormone végétale). Un exemple assez typique est la production d'acide citrique à partir de mélasse par le champignon Aspergillus niger. Cet acide est utilisé comme additif alimentaire à des fins de conservation ou d'acidification des produits alimentaires manufacturés.
Les biocarburants
Le bioéthanol est de plus en plus utilisé comme carburant pour les voitures, sa production fait appel à des cellulases provenant d'espèces de Trichoderma ou d'Aspergillus pour décomposer les déchets cellulosiques agricoles en sucres. Cela a permis le développement de biocarburants dits de deuxième génération qui ne concurrencent pas les cultures destinées à l'alimentation humaine et animale. Au lieu d'utiliser l'amidon des aliments, on va utiliser dans ce cas les déchets agricoles (par exemple les tiges, les feuilles) qui sont valorisés en les décomposant en sucres par l'action des cellulases fongiques, puis ils sont fermentés en éthanol par des levures. Le développement récent de voitures électriques alimentées par des piles à combustible à l'éthanol devrait contribuer à maintenir l'intérêt pour la production de bioéthanol à long terme.
La biolixivation
La biolixiviation est l'extraction des métaux de leurs minerais (par exemple cuivre, le zinc, le plomb, l'arsenic, l'antimoine, le nickel, le molybdène, l'or, l'argent et le cobalt) par l'utilisation d'organismes vivants, notamment des bactéries et plusieurs espèces de mycètes (des Aspergillus et des Penicillium par exemple). La consommation industrielle de métaux et de minéraux a considérablement augmenté au cours des dernières décennies. Le besoin croissant de matériaux électroniques, notamment ceux utilisés dans les ordinateurs, les téléphones portables et les télévisions, dépend fortement d'un large éventail de ressources métalliques et minérales. Parmi ces "éléments de technologie électronique" figurent le cobalt, les métaux du groupe du platine, le sélénium. Certains de ces éléments peuvent être difficiles à récupérer par les procédés d'extraction minière conventionnels et ne peuvent être trouvés en quantités importantes que dans un petit nombre de lieux géographiques.
La croissance des mégapoles très peuplées a également exacerbé les problèmes de recyclage et de récupération des métaux et a donné naissance au concept d'"exploitation minière urbaine", c'est-à-dire la récupération d'éléments minéraux importants à partir des déchets urbains. Les champignons (souvent de concert avec des bactéries) sont donc mobilisés à la fois pour l'extraction dans des écosystème naturel et la récupération à partir de déchets électroniques de métaux et de minéraux. Dans les nombreuses initiatives mondiales conçues pour améliorer la sécurité globale de l'approvisionnement de ces métaux tout en minimisant l'impact environnemental, le bio-traitement microbien est considéré comme un élément essentiel.
La mycoremédiation
Dans certains cas, les saprophytes sont capables de dégrader ou d'inactiver des substances chimiques pouvant avoir un impact néfaste sur la santé humaine et animale. Leur utilisation dans des stratégies de remédiations des zones polluées est de plus en plus envisagée : on parle de mycoremédiation. Les champignons possèdent la capacité biochimique et écologique de dégrader les produits chimiques organiques de l'environnement et et notamment certains polluants (métaux, hydrocarbures et radionucléides), soit en le modifiant chimiquement, soit en influençant leur biodisponibilité chimique.
Un autre exemple marquant est la découverte de la capacité de dégradation du polyuréthane de l'espèce fongique Pestalotiopsis microspora. Cette espèce endophyte fut isolée à partir de tiges de plante dans la partie ouest de la forêt amazonienne en Equateur par un groupe d'étudiants chercheurs dans le cadre de d'une expédition de l'Université de Yale. C'est la première espèce de champignon trouvée, qui soit capable de dégrader le polyuréthane en conditions d'anaérobie. Cela fait de ce champignon un candidat potentiel pour un projet de bioremédiation impliquant de grandes quantités de matière plastique.
Les mycomatériaux
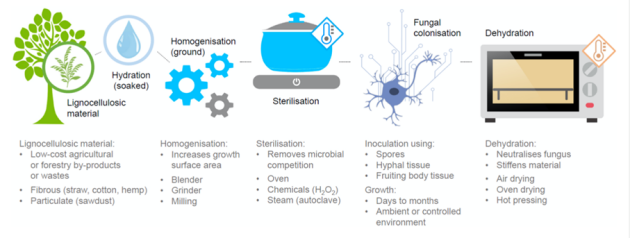
Les champignons sont également de plus en plus exploités pour générer divers types de matériaux. Le plus souvent, on utilise le mycélium pour lier des sous-produits de l'agriculture, tels que les copeaux de bois ou des déchets de maïs, afin de produire des matériaux durables, à base biologique et 100 % compostables. Le procédé est simple : les sous-produits ou déchets agricoles sont déshydratés, broyés et stérilisés. Ils sont étalés dans des moules et inoculés par des mycètes. C'est à cette étape qu'il faut faire preuve de patience car le mycète doit croître en agglomérant les particules végétales. Cela peut prendre plusieurs semaines. L'ensemble est ensuite déshydraté ce qui a pour résultats de neutraliser le champignon.
(crédits https://www.sciencedirect.com/science/article/pii/S0264127519308354#f0010)
Les composites à base de mycélium constituent une classe émergente de matériaux bon marché et durables sur le plan environnemental, qui suscite un intérêt croissant en matière de recherche et de commercialisation en Europe et aux États-Unis pour des applications dans le domaine de la construction. Les composites de mycélium ont des propriétés matérielles personnalisables en fonction de leur composition et de leur procédé de fabrication et peuvent remplacer les mousses, le bois et les plastiques pour des applications telles que l'isolation, les lambris, les revêtements de sol, les armoires et autres meubles.
En raison de leur faible conductivité thermique, de leur forte absorption acoustique et de leurs propriétés de sécurité incendie supérieures à celles des matériaux de construction traditionnels, tels que les mousses synthétiques et les bois d'ingénierie, ils sont particulièrement prometteurs en tant que mousses d'isolation thermique et acoustique.
Ce matériau à base mycélienne constitue aussi une alternative durable au polystyrène ou à certains plastiques. Une célèbre entreprise suédoise a d'ailleurs opté pour ce type d'emballage beaucoup plus écoresponsable.
Mycopesticides
Il est possible d'utiliser certains mycètes en agriculture notamment pour protéger les plantes cultivées contre certains agresseurs qui occasionnent des pertes de rendements ou mettent en péril la qualité des aliments. On parle de lutte biologique lorsqu'on utilise un mycète (ou un autre organisme) vivant. On peut parfois utiliser des extraits ou des molécules issues de mycètes pour la protection des cultures, on parle alors de biocontrôle.
Il est ainsi possible de déployer au champ des mycètes qui vont parasiter des insectes préjudiciables pour les cultures. On parle de mycoinsecticides. Certains mycètes ont aussi des propriétés nématicides en s'attaquant et tuant à ces vers ronds qui occasionnent des dégâts importants sur les plantes. Cela concerne des mycètes capables de produire des pièges (des filaments adhésifs, des structures en lasso) pour capturer les nématodes et ensuite s'en nourrir.
https://commons.wikimedia.org/wiki/File:Kecoa.jpg
https://microbewiki.kenyon.edu/index.php/File:Ring_trapping-2.jpg
et Franck Bastide (IRHS – Angers)
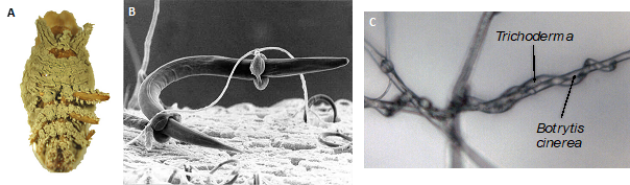
Un autre exemple d'hyperparasitisme microbien concerne l'utilisation du champignon Trichoderma qui est l'agent actif de plusieurs biofongicides commercialisés. Plusieurs espèces de ce genre fongique sont des mycoparasites efficaces, c'est à dire qu'ils sont capables de parasiter et de tuer d'autres mycètes notamment des mycètes pathogènes des plantes. Les filaments de Trichoderma s'enroulent autour de leur proie avant de s'en nourrir. Déployer ce genre de mycètes dans les cultures doit permettre de réduire la menace des ces champignons phytopathogènes
Les perspectives industrielles
À l'avenir, la biotechnologie fongique devrait être fortement influencée par la recherche dans le nouveau domaine de la biologie synthétique, qui implique la construction de systèmes biologiques artificiels pour la recherche et pour des applications en ingénierie et en médecine. Une équipe internationale de collaborateurs travaille actuellement à la production de levures avec des génomes synthétiques et ces organismes devraient avoir un potentiel biosynthétique accru. À l'avenir, il est probable qu'un plus grand nombre de produits pharmaceutiques, de produits chimiques et d'enzymes seront fabriqués dans ce type de levure ou d'autres plateformes de production.
Par ailleurs, il y a un réel intérêt à rechercher de nouveaux métabolites secondaires (MS) fongiques qui sont souvent très originaux avec des activités biologiques diverses. L'intérêt de rechercher de tels métabolites est d'autant plus important que les produits d'origine naturelle présentent souvent une plus grande diversité structurale que les composés issus de synthèse en laboratoire. La nature reste donc la plus inventive et imaginative.
Pour cette prospection de nouveaux métabolites, la stratégie la plus classique consiste à prélever des échantillons dans des environnements spécifiques, par exemple dans des environnements extrêmes car on augmente les chances de travailler sur des mycètes encore inconnus ou peu du moins pas classiquement étudiés. Ces prélèvements sont ensemencés sur des milieux de cultures adaptés aux champignons et mis à incuber. Les mycètes qui se multiplient à partir de ces échantillons sont isolés et les composés issus de leur culture sont testés pour diverses activités biologiques spécifiques. Cette méthode a des limites évidentes. Tout d'abord, on ne prend pas en compte tous les mycètes qui ne sont pas cultivables sur des milieux synthétiques. Ensuite, beaucoup de gènes codant des métabolites secondaires sont regroupés physiquement sur le génome dans ce qu'on appelle des clusters. Il apparaît que plusieurs de ces clusters de gènes ne s'expriment pas dans des conditions de cultures standards, on dit qu'ils sont silencieux ou encore cryptiques. Un des leviers utilisés pour faire exprimer le maximum de ces gènes est la mise en place du dispositif OSMAC (one strain-many compounds) qui vise à cultiver le même isolat sous une large gamme de conditions. On joue notamment sur la température ou encore la salinité des milieux. Une autre alternative est d'exposer les mycètes à des drogues qui perturbent le remodelage de la chromatine puisque les régulations épigénétiques peuvent être responsables de l'inhibition d'expression de ces clusters de gènes.
Une deuxième méthode dite génomique vise à séquencer les génomes des mycètes isolés et de rechercher spécifiquement les fractions de séquences correspondant aux clusters codant des MS. Ensuite, par ingénierie génétique, il est possible de modifier directement des portions d'ADN de l'organisme porteur de ces gènes, par exemple introduire un promoteur fort en amont pour permettre la synthèse du métabolite. Une autre alternative consiste à introduire ces gènes dans un organisme fongique modèle plus facilement manipulables (par exemple des Aspergillus ou des levures) pour faire exprimer ces gènes et permette la production du métabolite correspondant (on parle alors de production hétérologue).
Enfin, avec les progrès des techniques de séquençage, une méthode plus récente dite métagénomique a vu le jour. Le gros avantage de cette méthode, qui reste par ailleurs délicate, à mettre en œuvre, est qu'elle permet d'identifier des MS issus d'organismes non cultivables. L'ADN dans ce cas est directement extrait à partir de l'échantillon prélevé dans l'environnement (sans passer par une étape de culture et d'isolement fongique sur milieu synthétique). Les fragments d'ADN comprenant un cluster de MS peuvent ensuite être introduits et exprimés dans des organismes hôtes en utilisant par exemple des vecteurs particuliers, tels que des BAC ou des cosmides ou encore des FAC, qui peuvent prendre en charge de très gros fragments d'ADN.