Hydratation du but-1-ène
On réalise l'hydratation du but-1-ène en milieu acide On va étudier, dans un premier temps, les différentes étapes du mécanisme réactionnel qui a lieu en trois étapes. L'équation bilan est la suivante :

Question
Nommer le produit formé, quelle est sa fonction chimique ?
Le produit est le butan-1-ol et il a une fonction alcool.
Question
De quel type de réaction s'agit-il ? Justifier.
Il s'agit d'une réaction d'addition. Il y a eu addition d'une molécule d'eau sur l'alcène.
Question
La réaction ne se fait pratiquement pas si le milieu n'est pas acidifié, quel est le rôle des ions H+(aq) ?
Les ions H+(aq) ont un rôle de catalyseur.
Question
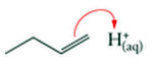
Sachant que la première étape du mécanisme concerne le but-1-ène et l'ion H+(aq), choisir, en argumentant, la bonne représentation de cette première étape.

L'alcène est riche en électrons (la double liaison) et va jouer le rôle de site donneur d'électrons.
L'ion H+ est une espèce déficitaire en électrons et va jouer le rôle d'accepteur d'électrons.
Par conséquent, les flèches courbes tracées d'un mécanisme réactionnel vont du site donneur au site accepteur de doublet d'électrons.
Question
Il se forme alors cet intermédiaire réactionnel :
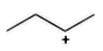
Ce dernier se comporte-t-il comme un site donneur ou accepteur dans la deuxième étape ?
Puisque le carbone est chargé positivement, il est déficitaire en électrons et il se comportera comme un accepteur de doublet d'électrons.
Question
Cet intermédiaire va réagir avec l'eau. Donner le schéma de Lewis de la molécule d'eau et indiquer quel atome est impliqué dans la deuxième étape.

La deuxième étape implique un site donneur de doublet d'électrons donc c'est l'atome d'oxygène qui sera impliqué.
Question
On obtient alors le composé ci-contre :
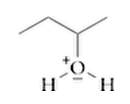
Schématiser la troisième étape pour arriver au produit attendu.
Question
Pourquoi cette étape valide-t-elle la réponse à la question 3 ?
Cette étape valide bien le fait que les ions H+(aq) ont un rôle de catalyseur car ils sont consommés dans la première étape et récupérés dans la troisième. Au final, leur concentration reste identique.







