Représentation plane
Formule brute
La formule brute donne la nature et le nombre d'atomes dans une molécule. Le symbole de l'élément est indicé en bas à droite par le nombre d'atomes de cet élément présent dans la molécule. Le nombre 1 est sous-entendu.
Par exemple une molécule de méthane a pour formule brute
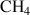 , elle contient 1 atome de carbone et 4 atomes d'hydrogène.
, elle contient 1 atome de carbone et 4 atomes d'hydrogène.
Formules développées
La formule brute ne donne aucune indication sur la répartition des atomes dans la molécule. La formule développée précise cette répartition ainsi que les liaisons covalentes reliant les atomes.
Exemple :
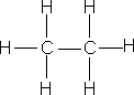
On utilise la symbolisation de Lewis : la liaison covalente simple est représentée par un trait tandis qu'une liaison covalente double est représentée par deux traits parallèles et de même longueur. Un doublet libre y est également représenté par un trait. Cette représentation est plane et ne rend pas compte de la géométrie de la molécule.
Par exemple, les formules développées de l'éthane de formule brute
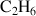 et du dioxyde de carbone
et du dioxyde de carbone
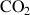 .
.
Formules semi-développées (condensées on combinées)
Dans la formule combinée d'une molécule, les atomes d'hydrogène reliés à un même carbone sont rassemblés à coté de ce carbone. Les liaisons entre atomes de carbone et d'hydrogène sont sous-entendues. Par contre les liaisons entre carbones sont précisées.
Exemple :
La formule de l'éthane est :
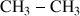
La formule condensée, quant à elle, ne précise pas les liaisons simples entre carbones, ce qui donne pour l'exemple précédent :
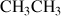
Formules topologiques
Cette représentation ne précise pas :
les atomes de carbone
les atomes d'hydrogène reliés à un atome de carbone
les liaisons entre un atome de carbone et un atome d'hydrogène.
Exemple :
La molécule de butan-1-ol ayant pour formule combinée :
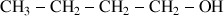 a pour formule topologique :
a pour formule topologique :
Les divers modes de représentation plane des molécules
L'animation Flash suivante illustre l'écriture de la formule du Propane de 4 façons différentes :
formule brute
formule développée
formule combinée
formule topologique






